欢迎光临吉康旅!
*仅供医学专业阅读参考
每天1分钟,给你肿瘤圈的专业“讲堂”!(如需文献原文,可加小编微信获取)
关键点
:国产贝伐单抗生物类似药疗效和安全性与贝伐单抗相似,有望成为非鳞状一线治疗的新选择
CLIN RES:新辅助免疫治疗局部晚期可切除头颈部皮肤鳞状细胞癌安全性好,病理缓解率高
新药:国产抗HER2 ADC获得HER2阳性乳腺癌突破性疗法认定
新药:中国首个MUC1 ADC获批临床
01
:国产贝伐单抗生物类似药疗效和安全性与贝伐单抗相似,有望成为非鳞状一线治疗的新选择
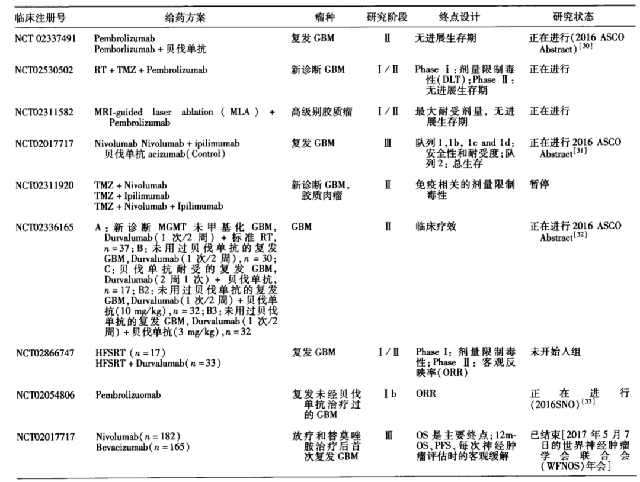
最近,一项比较贝伐单抗生物仿制药与贝伐单抗一线治疗不可切除的转移性或复发性非鳞状非小细胞肺癌()的 III 期研究发表。结果显示,在中国晚期或复发性非鳞状细胞癌患者中,其疗效和安全性与贝伐单抗相似,有望成为一线治疗的新选择。
在这项多中心 RCT 中,649 名 IIIB-IV 期患者按 1:1 随机分配接受(n=325) 或贝伐单抗(n=325)15 mg/kg IV,联合紫杉醇/卡铂) 4-6个周期,随后维持单药治疗直至疾病进展、不可接受的毒性或死亡。中位随访时间为13.6个月。
贝伐单抗组和贝伐单抗组的客观缓解率 (ORR) 分别为 48.5% 和 53.0%。两组的疾病控制率(DCR)、中位缓解持续时间(DoR)、中位无进展生存期(PFS)、中位总生存期(OS)和1年OS率均无显着差异。两组之间在安全性和免疫原性方面没有临床意义的差异。
02
CLIN RES:新辅助免疫治疗局部晚期可切除头颈部皮肤鳞状细胞癌安全性好,病理缓解率高

最近,一项旨在调查新辅助免疫治疗治疗局部晚期可切除头颈部鳞状细胞癌(CSCC-HN)安全性的初步 II 期临床研究发表在 CLIN RES 上。结果表明,局部晚期CSCC-HN的新辅助免疫治疗是安全的,并且达到了较高的病理缓解率。病理反应与炎症性肿瘤微环境有关。
符合根治性手术条件的新诊断或复发 III-IVA 期 CSCC-HN 患者接受了 2 个周期的新辅助 PD-1 抑制。在入组的 20 名患者中,有 7 名复发。根据实体瘤疗效评价标准1.第1版(v1.1),仅6例患者(30%)获得部分缓解,14例患者(70%)获得病理完全缓解缓解(pCR;n = 11) 或主要病理缓解(MPR;n = 3))。新辅助治疗期间或之后未发生严重不良反应。中位随访时间为 22.@ > 6个月时进展死亡1例,无病死亡1例,复发2例,12个月DSS、DFS、OS率分别为95%、89.5%、95%。
03
新药:国产抗HER2 ADC获得HER2阳性乳腺癌突破性疗法认定
近日,中国国家药品监督管理局(NMPA)药品审评中心(CDE)网站显示,刚刚获批上市的国内首个原创抗体偶联药物(ADC)新药已获批上市。 “抗HER2单克隆抗体-MMAE偶联物”)正式纳入突破性治疗类别,适应症为既往接受过曲妥珠单抗和紫杉类药物治疗的HER2阳性晚期肝转移乳腺癌患者。该适应症正在中国进行III期临床试验。
这是 的第三个突破性疗法认定。2020年9月和2020年12月,该治疗尿路上皮癌的药物先后获得美国食品药品监督管理局(FDA)和中国食品药品监督管理局的突破性疗法认证,成为美国和中国首个突破性疗法。也是迄今为止唯一获得FDA突破性疗法认定的国产ADC药物。
04
新药:中国首个MUC1 ADC获批临床
近日,杭州多喜生物科技有限公司旗下的注射用1类抗体偶联物(ADC)重组人源化抗MUC1单克隆抗体偶联剂获得临床试验默示许可。这是国内首个获得临床批准的MUC1。ADC新药。MUC1 是一种高分子量糖蛋白,在肿瘤组织中具有异常表达和极性缺失。该蛋白与细胞粘附、免疫调节等多种生物学功能密切相关,被认为是抗肿瘤免疫的理想靶点之一。
参考:
1.石毅、雷凯、贾毅等。with () as -line for with , , or non- non- non-non-non-non-non-non-cell lung: A , , -, III . (伦敦)。2021 年 6 月 2 日 9.
2.@> 中的 II,头颈细胞。
3.
4.
本文首发:医学肿瘤频道
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话