欢迎光临吉康旅!
自去年6月首个MET TKI抑制剂在中国上市以来,多种针对MET靶点的药物将在今年年底和明年初进入中国临床。相信MET将成为下一个渐开线目标。为了更好地了解该靶点的后续系列进展,本专题基于中国医学科学院肿瘤医院王杰教授团队在&杂志上发表的文件《MET-and : A》 2022年3月10日[1]让我们梳理一下这次定位的进度。
1.MET目标介绍
间充质-上皮转化 (MET) 原癌基因——受体酪氨酸激酶或肝细胞生长因子 (HGF) 受体——属于受体酪氨酸激酶 (RTK) 家族,并与其配体 HGF(HGF/MET 轴)相关联在正常生理条件下参与转导途径并调节基本细胞过程。研究表明,多种癌基因改变,包括突变、MET 扩增、MET 过表达、染色体重排和融合,会导致 HGF/MET 轴的失调,从而导致肿瘤发生。除了其生理和病理作用外,MET 是对靶向治疗(表皮生长因子受体 [EGFR] 和血管 EGFR[] 抑制剂)产生耐药性的常见机制。基于这一证据,HGF/MET 轴已被探索为不同癌症类型药物开发的治疗靶点。在过去的十年中,已经开发出几种 MET 抑制剂,包括单克隆抗体、双特异性抗体 ()、抗体-药物偶联物 (ADC) 和小分子药物,并处于临床评估的不同阶段。这些药物可以作为单一疗法使用,也可以与其他药物联合用于各种肿瘤。 2020年3月,日本厚生劳动省批准用于治疗MET外显子14跳跃突变的不可切除、晚期或复发性非小细胞肺癌()。同年5月,美国FDA批准卡马替尼用于治疗MET外显子14跳跃突变的成年患者。此外,2021年6月,国家药品监督管理局获批用于治疗MET外显子14跳跃突变的非小细胞肺癌。这篇文献综述总结并概述了各种MET抑制剂(单克隆抗体和小分子抑制剂)在不同肿瘤类型中的临床疗效。
2.非小细胞肺癌
22 项研究报告了各种 MET 抑制剂在不同 MET 异常患者中的临床结果。四项研究包括 MET 外显子 14 跳跃突变的患者,其余研究包括 MET 扩增或过表达或 MET 外显子 14 跳跃突变/MET 扩增的患者。 12 项研究报告了单药治疗,10 项研究报告了联合治疗。大多数研究报告了涉及克唑替尼的单药治疗。
2.跳跃
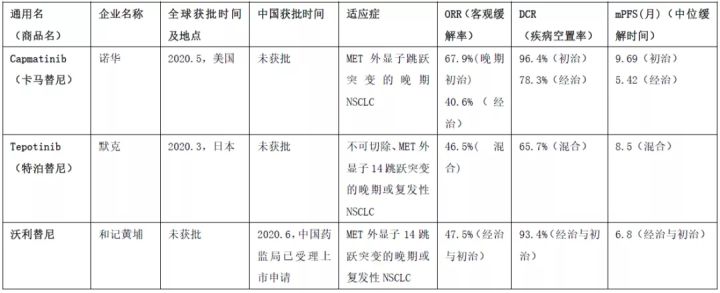
MET 外显子 14 跳跃突变被认为是独立的驱动突变,通常与其他驱动突变(如 EGFR、ALK、ROS1) 相互排斥,并且与预后不良有关。MET 也被报道为外显子14 个跳跃突变代表了一种临床上不同的分子亚型,有助于个体化治疗的患者分层。已经报道了针对 MET 外显子 14 跳跃突变的靶向治疗的许多进展。4 种 MET TKI(克唑替尼、、 和 )的结果已有文献报道,见下表。
另外:除上述数据外,还有一些未列出或未更新的数据如下表[2][3][4][5]所示,我们看到更多关于克唑替尼治疗疗效的数据,但数据稳定 性能较差,研究间结果差异较大; 通过增加样本量进一步证实了对跳跃患者的疗效;双抗体药物也开始在跳绳中显示疗效,患者还在招募中。
2.2 EGFR TKI 耐药 MET 扩增
由于 MET 和 RTK (EGFR) 信号通路之间的串扰,MET 激活会对 EGFR TKI 的有效性产生负面影响,因为 EGFR 激活会导致 MET 激活增加,反之亦然。 MET 扩增通过旁路激活促进下游信号传导,从而避免 EGFR TKI 引起的细胞死亡。因此,MET扩增是EGFR TKI的重要耐药机制。一线/二线EGFR TKI耐药发生率为5-21%,一线治疗后约15%,晚期奥希替尼耐药后约19%。此外,可以想象 MET 激活在 EGFR TKI 治疗后 MET 扩增的患者和未接受治疗的患者之间可能不同。因此,在对 EGFR TKI 获得性耐药的患者中使用 MET 抑制剂可能需要与未接受过治疗的患者不同的策略。将 MET TKI 与 EGFR TKI 结合可能是解决 MET 驱动的 EGFR TKI 耐药性的方法。文中提到的这类研究。
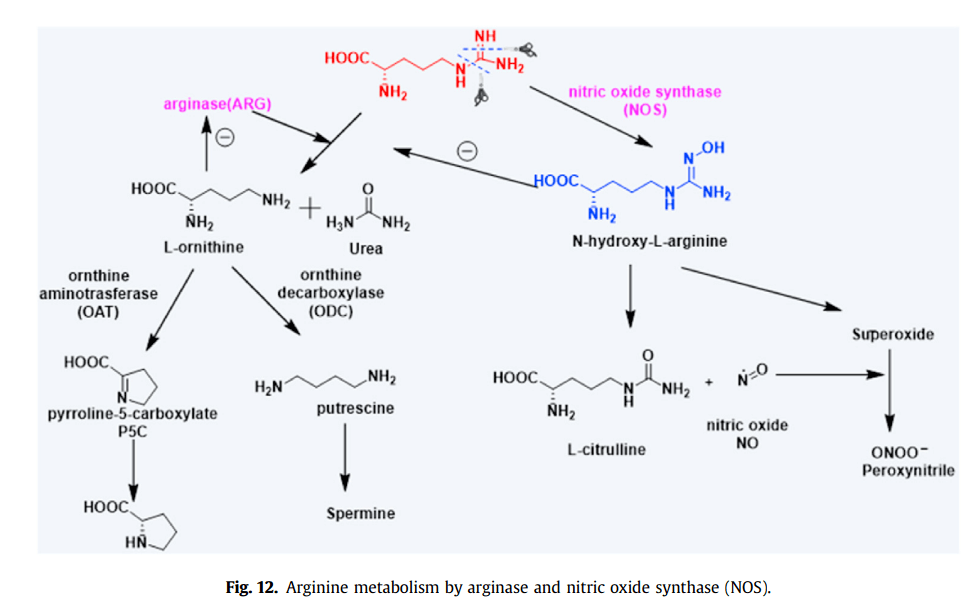
2.3 初级 MET 扩增/过表达
具有初级 MET 扩增(高水平,即 MET/CEP7 比率 ≥ 5))的肿瘤主要依赖于 MET 信号通路的生长。发现这些扩增<1-5%,表明预后差。此外,文献表明,与低水平的 MET 扩增相比,较高水平的 MET 扩增更有可能表明对 MET 的致癌依赖性,因此是一种亚型。另一方面,在没有已知的 MET 扩增的情况下,MET 过表达在依赖驱动程序的环境中是 MET TKI 益处的不良预测因子。然而,作为致癌驱动因素的 MET 过表达或原发性 MET 扩增仍存在争议。多项试验已将 MET 用于 MET 扩增抑制剂。
在1001研究和mono-1研究中探讨克唑替尼和卡马替尼单药治疗对MET扩增的疗效,发现高MET扩增的患者具有更高的ORR和PFS。此外,其他MET TKI的探索也在进行中,如研究等。
2.4 种新的 MET 抑制剂
除MET TKI外,其他类型药物、ABBV-399等数据不断披露。
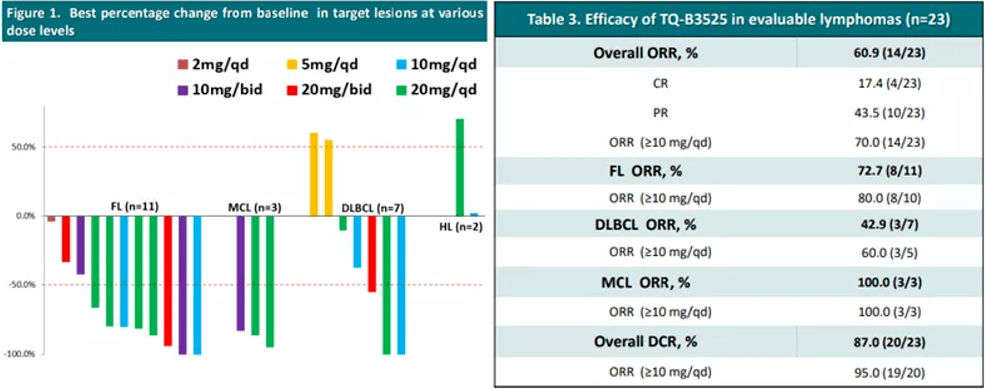
PS:截至本文发表,艾伯维的ADC药物-v)已获得各FDA突破性药物认定,疗效数据如下图[6]。我们看到,虽然 MET TKI 还在为哪些检测方法而苦苦挣扎,但 ADC 药物已经率先确定了使用 IHC 检测来指导治疗。
其他肿瘤类型见下一期。 . . . . . 参考 ^董 Y、徐 J、孙 B、Wang J、Wang Z. MET- and : A .摩尔。 2022 年 3 月;26(2):203-227.doi: 10. 1007/-021--w. Epub 2022 年 3 月 10 日。PMID: .^2021 ASCO 9020^Moro- D, N, Pérol M, Mazières J,奥托 J,PJ,R,M,G,SD,Barlési F,B,I,R,Bota S,C,V,V,G,A,De F,M,Hoog-N,G。
在 c-MET- 或 ROS1- 中:AcSé II。安。 2019 年 12 月 1 日;30(12):1985-1991.doi: 10. 1093 //.PMID: .^ L, R, M, D'Incà F, C, A, A, L, D, DL, de F, G, A, C, D, F, F, E, G, F, C, Bria E, Alì G, R, A, G, Crinò L, F. in MET- 或 ROS1- 非细胞肺 (): A II, , , 双臂。
临床研究。 2019 年 12 月 15 日;25 日(24):7312-7319.doi:10.1158/1078-0432.CCR-19-0994.Epub 2019 年 8 月 15 日。PMID:.^2021 WCLC in Non Cell Lung ()与 MET 外显子 14 ( ) : 来自 ^2021 WCLC : OA15.04
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话