欢迎光临吉康旅!
EGFR突变是肺癌患者常见的突变类型。根据突变位点的不同,可分为经典突变(或外显子21)和罕见突变。目前,对于经典突变,临床推荐使用第三代EGFR-TKI 一线治疗。然而,作为一种靶向药物,奥希蒂尼始终面临着耐药性的命运。奥耐药性的治疗一直是临床研究的热点。今天,我将向大家报告,首例肺腺癌脑转移患者在奥西汀一线耐药后,通过两次化疗“再致敏”,在奥西汀的三场战役中取得了三场胜利。到2021 4月,患者的总生存期已达到40个月,生活质量良好
诊断:晚期肺腺癌伴脑转移+egfr突变
患者为57岁女性,因刺激性咳嗽和胸痛入院,无家族遗传史
实验室检查:
血常规、肝肾功能、电解质试验均正常。血清癌胚抗原(CEA)水平为14
影像检查:
胸部计算机断层扫描(CT)显示右肺上、中叶有不规则的高密度病变,纵隔有多个肿大的淋巴结,右胸有胸腔积液。最大病变的边界约为3
病理检查:
胸膜液薄层细胞学诊断为肺腺癌,胸膜液中发现EGFR突变
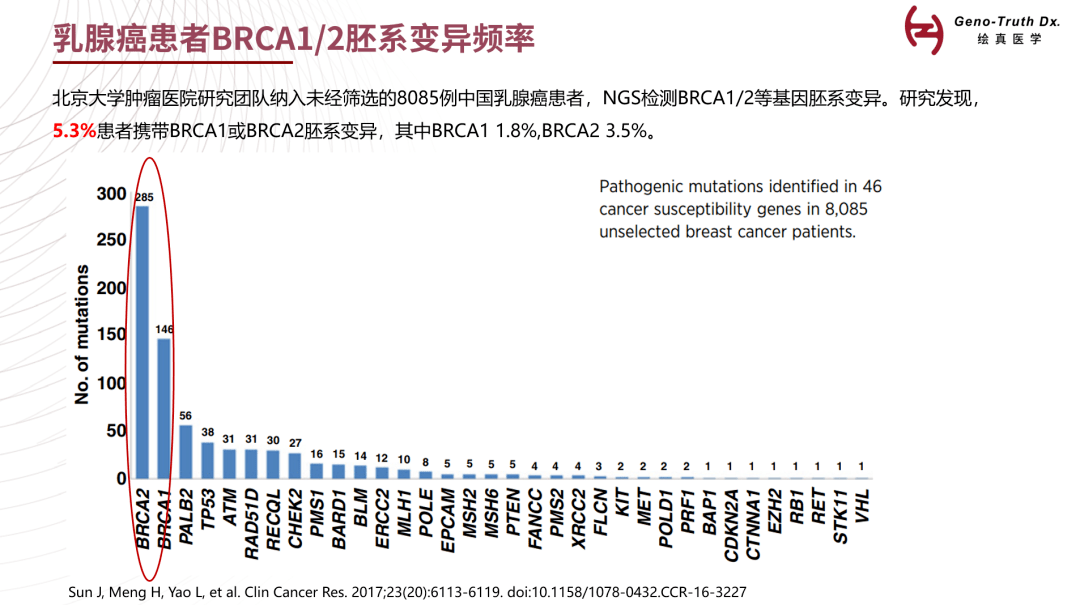
最终诊断:
晚期肺腺癌伴多发淋巴结、胸膜和脑转移,临床分期为IVA期,伴有EGFR突变
赢得了三场战争和三场胜利,实现了完美的40个月OS
1.用进行一线治疗:
2018年1月,使用(80mg)进行一线治疗。治疗期间,血清肿瘤标志物和CEA水平下降。同时,CT扫描显示肿瘤病灶减少(图1c)。治疗5个月后,脑转移消失(图1D),多发性肺部病变减少,表明西地尼具有临床益处
2018年12月,在使用治疗11个月后,肺部CT扫描显示右侧胸膜出现多个新病灶(以前从未发现),表明疾病进展(PD)(图2b)。通过血浆分析,发现EGFR突变已消失。所以被停止了
二线化疗致敏:
在对奥西替尼一线耐药后,进行培美曲塞+顺铂三个疗程的化疗。2019年3月,图像显示原发病灶稳定,但胸膜转移灶扩大并略有增加。第二次血浆检测采用arms-PCR方法,再次发现EGFR突变
奥昔替尼三线第二次挑战赛
因此,在第三线治疗(再次激发)中第二次使用了。治疗2个月后,胸膜癌病灶几乎消失(图2D),表明培美曲塞+顺铂化疗成功地再次致敏,肿瘤对奥西替尼再次敏感。然而,使用约半年后,2019年9月,胸膜转移再次开始扩大,疾病再次进展,但患者拒绝接受基因检测
四线化疗致敏:
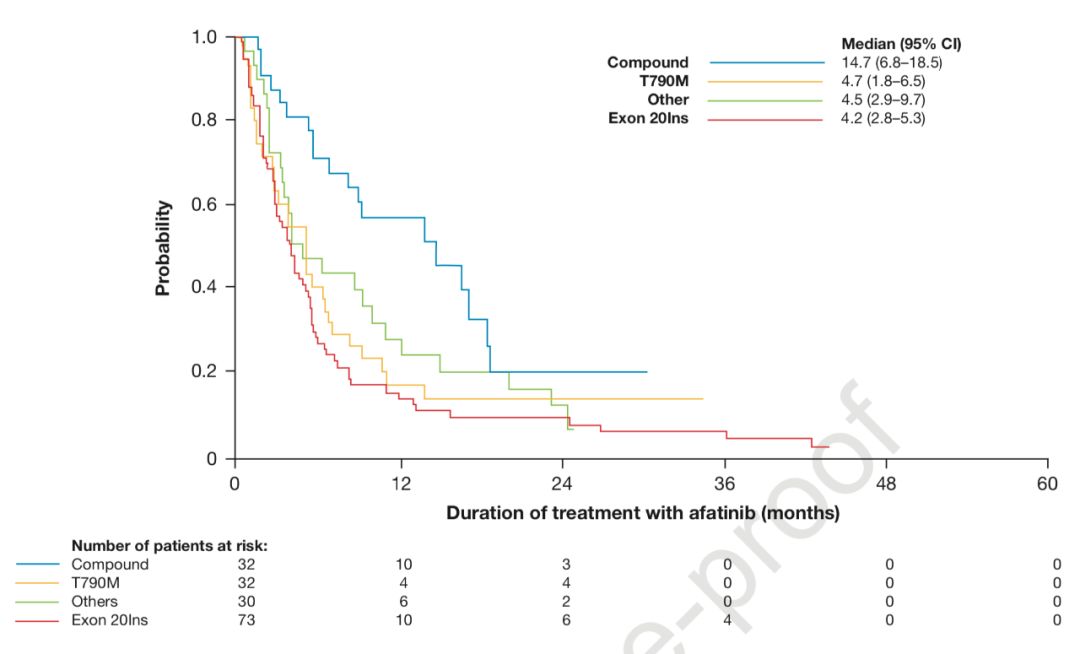
因此,患者接受了2个周期的白蛋白-紫杉醇联合顺铂化疗(q3w)。影像学显示原发病灶稳定,但右侧胸膜进展
奥昔替尼五行三大挑战:
2019年10月14日,患者在化疗进展后接受了第三次奥西替尼挑战(每天一次80毫克)。40天后,常规胸部CT扫描显示胸膜病变再次消失,原发病灶稳定,转移性脑病未复发。到2021 4月,患者的总生存时间为40个月,生活质量良好
治疗期间肿瘤标志物CEA的变化:
对案件的六点思考
的耐药策略之一-交替化疗
目前,已成为EGFR突变型肺癌患者的一线标准治疗药物。通过研究,一线使用可以实现无进展生存PFS和总生存月数。然而,作为一种靶向药物,的一个大厄运是耐药性
解决耐药性问题的机制之一是化疗。在之前的一项研究中,纳入了17名再次挑战的患者,先前治疗线的中位数为5。大多数患者(14例)在接受激发前进行了化疗,4例进行了免疫治疗。第二次激发的Orr和DCR分别为33%和73%。中位PFS4.>1个月,中位OS为9个月
目前,临床上对耐药机制的研究较多。许多耐药患者可以通过基因检测找到目标突变,然后进行靶向治疗,从而获益更多。如果的耐药性通过基因检测,并且没有可用的靶向药物,理论上应积极转为化疗
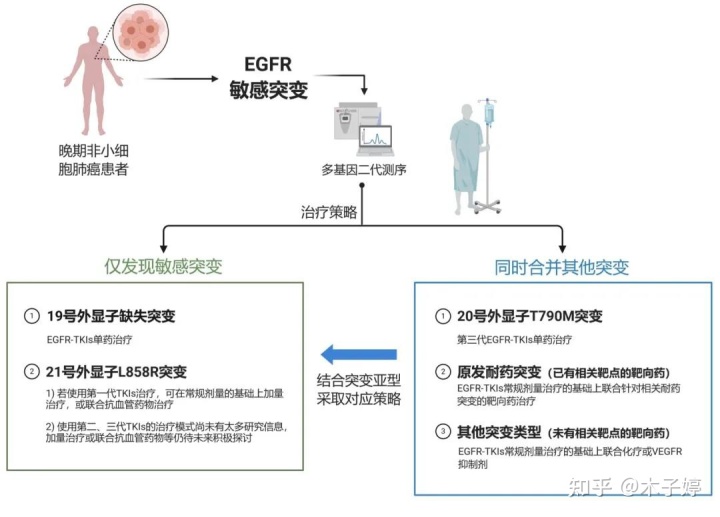
化疗增敏和TKI再激发机制
2019年,宋勇/吴一龙教授的团队公布了下一代TKI吉非替尼()挑战赛的测试数据。第一项前瞻性研究结果证实,化疗后使用TKI可致敏。此外,一些临床研究指出,EGFR-TKI在治疗晚期EGFR突变耐药患者后更有效,然后使用几个周期的化疗,然后重新开始EGFR-TKI治疗。从EGFR-TKI停药到重启的时间间隔称为EGFR-TKI的“停药期”。为什么肿瘤可以在“停药期”通过化疗对EGFR-TKI再致敏?在临床实践中,关于相关机制的讨论很多,其中被广泛接受的说法是“此起彼伏”
在靶向治疗之前,EGFR突变的癌细胞在整个肿瘤细胞组中占很高的比例。因此,EGFR-TKI治疗后,大部分EGFR突变的肿瘤细胞被清除,其余为少数对EGFR-TKI耐药的癌细胞,逐渐成为优势群。因此,EGFR-TKI对EGFR-TKI具有耐药性
化疗通过细胞毒性而不是通过抑制EGFR途径杀死肿瘤。因此,联合化疗可以杀死许多对EGFR-TKI耐药的癌细胞,而对EGFR-TKI敏感的细胞可能会复活。当EGFR-TKI在化疗耐药后重新启动时,这构成了EGFR-TKI耐药后化疗的“致敏”机制
哪些患者在靶向耐药后容易进行化疗
靶向再激发的可能优势人群:两种靶向治疗之间的间隔≥ 7个月;21外显子突变女性;在两次试验中,EGFR的突变丰度较低;化疗药物培美曲塞
在本例中,患者被诊断为具有EGFR外显子21突变的肺癌患者,因此他在第一线接受了治疗。治疗11个月后的第一次PD,未发现EGFR突变,这间接反映了EGFR突变癌细胞不再是优势群体。因此,进行了化疗。经过两个疗程的化疗,血浆中再次出现EGFR外显子21突变,因此的挑战是成功的。不幸的是,患者在第三次使用治疗期间拒绝了随后的基因测试,这使得我们无法获得更多信息来更深入地了解这一现象。因此,我们期待着在未来进行更大样本量的多中心前瞻性研究
两者都是EGFR的经典突变,但EGFR和突变是不同的
EGFR突变和突变都是经典的EGFR突变,但现在越来越多的临床研究将分析这两种亚型。2020年第17届肺癌共识指出,对于晚期EGFR突变阳性阶段,需要细分EGFR敏感突变的两个亚型(外显子和外显子21)以及是否存在脑转移,并分别给予不同的治疗:对于突变,首选达科替尼、埃罗替尼+贝伐单抗和埃克替尼;对于外显子19突变,和是首选,而通常是推荐的。对于晚期EGFR突变,有必要进一步细分不同的突变亚型以进行精确的个体化治疗。因此,也有人提到,适合替代化疗的主要人群之一是外显子21突变
5.在靶向耐药后,通过化疗使其重新致敏。靶向再激发也适用于其他癌症
此前,临床试验数据发表在JAMA上。这项试验包括28名Ras和BRAF野生型晚期转移性结直肠癌(mCRC)患者,他们之前接受过包含伊立替康和西妥昔单抗的一线治疗方案,以及包含奥沙利铂和贝伐单抗的二线治疗方案,注册后,他们接受了
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话