欢迎光临吉康旅!
2020 年 1 月 21 日 / 生物谷 / -- 阿斯利康 () 和默克公司 ( & Co) 近日宣布,美国食品药品监督管理局 (FDA) 已接受(中文品牌名称:立普妥,通用名称:奥拉帕尼片) 和补充新药申请 (sNDA) 被授予优先审查。 sNDA 寻求批准一种新的激素制剂
2020 年 1 月 21 日 / 生物谷 / -- 阿斯利康 () 和默克公司 ( & Co) 近日宣布,美国食品药品监督管理局 (FDA) 已接受(中文品牌名称:立普妥,通用名称:奥拉帕尼片) 和补充新药申请 (sNDA) 被授予优先审查。 sNDA 寻求批准接受新激素药物、有害或疑似有害种系或体细胞同源重组修复基因突变 (HRRm) 治疗的转移性去势抵抗性前列腺癌 (HRRm) 患者。 FDA 已将 sNDA 的处方药用户费用法案()的目标日期指定为 2020 年第二季度。
目前,另一个也在 FDA 优先审查的 sNDA 正在寻求批准作为对铂类化疗和贝伐单抗一线治疗完全缓解或部分反应的患者的维持治疗( )晚期患者卵巢癌处于缓解期。 FDA 已指定 2020 年第二季度的目标日期。
基于 III 期试验结果的前列腺癌 sNDA 的优先审查。共有 387 名患有转移性去势抵抗性前列腺癌 ( ) 的男性参加了该研究,这些患者的肿瘤与 15 个参与同源重组修复 (HRR) 信号传导的基因 (BRCA 1/2、ATM 和其他突变在 11 个 HRRm 基因之一中)并且他的疾病在接受新的激素剂 (NHA) 后进展。该研究评估了相对于标准护理药物(恩杂鲁胺)或(醋酸阿比特龙)的疗效和安全性。
值得注意的是,该研究是第一项在选择生物标志物的前列腺癌患者人群中评估靶向药物的 III 期研究。
结果显示,BRCA 1/2 或 ATM 突变患者的主要终点影像学无进展生存期 (rPFS) 有统计学意义和临床意义的改善。具体而言,接受阿比特龙或恩杂鲁胺治疗的患者的影像学无进展生存期延长了一倍(中位 rPFS:7.4 个月 vs 3.6 个月),疾病进展风险显着降低 66%,或死亡(HR=0.34[95%CI:0.25-0.47],p<0.0001)。
此外,与接受阿比特龙或恩杂鲁胺治疗的患者相比,该研究在具有 HRRm 基因(BRCA 1/2、ATM 和其他 11 个 HRRm 基因)的患者中达到了 rPFS 的关键次要终点,与接受治疗的患者相比,放射学无进展生存期显着延长(中位 rPFS:5.8 个月 vs 3.5 个月),疾病进展或死亡风险显着降低 51%(HR =0.49[95 %CI:0.38-0.63], p<0.0001). 本研究中容性的安全性和耐受性与之前观察到的一致临床研究。
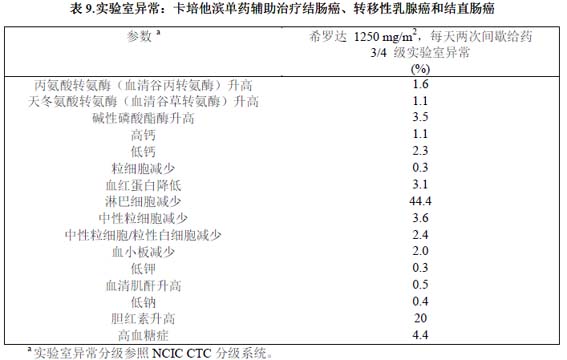
研究结果表明,除了为携带 BRCA 突变肿瘤的转移性去势抵抗性前列腺癌患者提供作为精准药物的实质性益处外,BRCA 之外的同源重组修复 (HRR) 的其他方面与该基因突变的肿瘤也起作用。研究验证了与该疾病同源重组修复相关的多个基因中 PARP 敏感性的概念,标志着首次使用分子标记物来识别转移性去势抵抗性前列腺癌和靶向药物治疗患者的第一项阳性 III 期研究。
目前,阿斯利康()和默克()也在探索其他前列腺癌试验,包括正在进行的 III 期试验,该试验评估阿比特龙联合作为一线疗法治疗有或没有 HRR 突变的患者。
是一种一流的口服多聚 ADP 核糖聚合酶 (PARP) 抑制剂,它利用肿瘤 DNA 损伤修复 (DDR) 途径中的缺陷优先杀死癌细胞,这种作用模式在DNA 损伤修复 多种肿瘤类型的缺陷潜力。

它是全球首个上市的PARP抑制剂,于2014年12月首次获得美国FDA批准。迄今为止,该药物已在全球65个国家获批用于铂敏感复发性卵巢癌的维持治疗(无论BRCA 状态)。该药物在美国、欧盟、日本、中国和其他一些国家被批准作为铂类化疗后缓解的 BRCA 突变( )晚期卵巢癌的一线维持治疗。此外,它在包括美国和日本在内的 44 个国家被批准用于先前接受过化疗的 HER2 阴性转移性乳腺癌,在欧盟,该适应症包括局部晚期乳腺癌。目前,其他司法管辖区正在审查卵巢癌、乳腺癌和胰腺癌的治疗方法。
阿斯利康与默克于 2017 年 7 月在肿瘤学领域达成全球战略合作,共同开发和商业化另一种用于治疗各种类型肿瘤的 MEK 抑制剂。在PARP抑制剂类别中,拥有最广泛、最先进的临床试验开发计划。目前,双方正在合作研究作为单一疗法以及联合疗法对多种肿瘤类型的治疗潜力。
在中国市场,()于2018年8月获批用于铂敏感复发性卵巢癌的维持治疗。这是中国市场上首个获批用于治疗卵巢癌的靶向药物,标志着中国卵巢癌的治疗进入了PARP抑制剂时代。 2019年12月再次获批用于BRCA突变晚期卵巢癌患者的一线维持治疗。受益于国家对药物创新的大力支持和急需新药审批的加快,成为国内首个获批用于卵巢癌一线维持治疗的PARP抑制剂。 2019年11月28日,纳入国家医保目录。 (生物谷)
原始来源:在美国用于 HRR--
免责声明: 本站关于疾病和药品的介绍仅供参考,实际治疗和用药方案请咨询专业医生和药师。

微信扫码◀
免费咨询电话