多吉美/索拉非尼是一线全身治疗药物的研究与实践
发布日期:2021-11-19 浏览次数:432
多吉美/索拉非尼是过去十年中唯一获批的晚期肝细胞癌(HCC)一线全身治疗药物。肿瘤对索拉非尼的耐药性一直是提高 HCC 患者生存率的主要障碍。
方法
我们将 THP-1 细胞极化为 M1 和 M2 巨噬细胞,进行了各种体外测定并开发了索拉非尼耐药异种移植模型,以研究肿瘤相关巨噬细胞 (TAM) 分泌的分子在 HCC 中对靶向治疗的抵抗作用。
结果
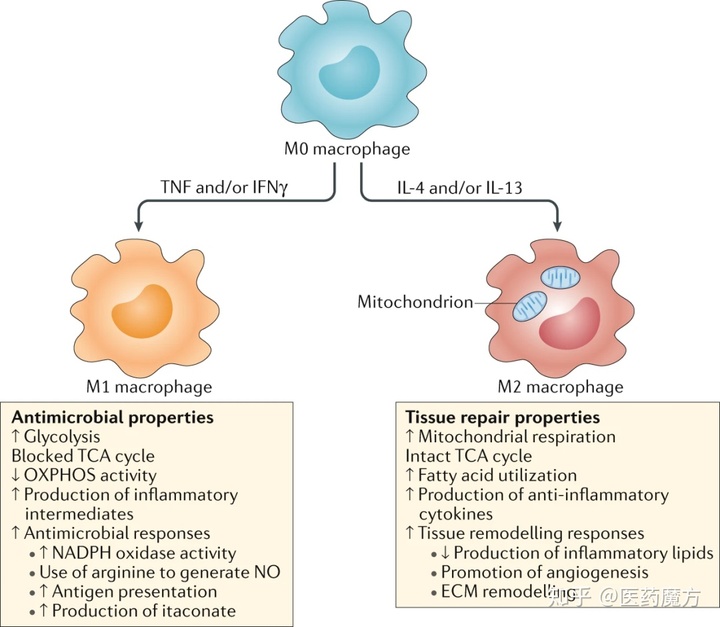
我们证明M2(不是M1)巨噬细胞不仅促进肝癌细胞的增殖、集落形成和迁移,而且通过分泌肝细胞生长因子(HGF)来维持肿瘤的生长和转移,这显着赋予了的肿瘤抗性HGF 激活肿瘤细胞中的 HGF/c-Met、ERK1/2/MAPK 和 PI3K/AKT 通路。肿瘤相关 M2 巨噬细胞在索拉非尼耐药肿瘤中的积累比例索拉非尼对体内肿瘤更敏感,并且产生丰富的HGF,HGF在化学上吸引更多的巨噬细胞从周围迁移过来,调节M2型巨噬细胞的分布,增加肝癌对Sola 抗性的影响。
综上所述
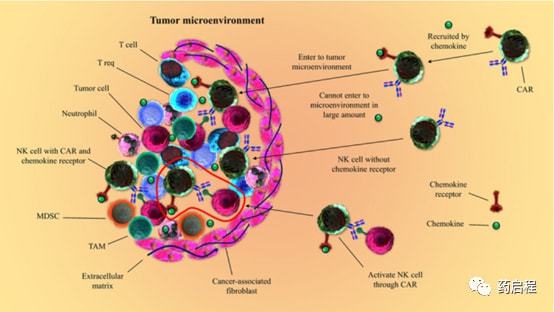
我们的发现为 HCC 中多吉美/索拉非尼耐药机制提供了新见解,并提供了一种通过将索拉非尼与强效 HGF 抑制剂(如卡博替尼)联合来改善一线全身治疗的方法。为开展新实验的基本原则提供了基础结果。
巨噬细胞是 TME 的主要成分,主要从血液循环单核细胞中招募,并驻留在细胞因子 CSF-1、趋化因子 CCL2、CCL9、 和骨膜蛋白中。留在肿瘤组织 (TAM) 中。TAM 有可能触发破坏性的肿瘤反应(抗肿瘤活性)或驱动肿瘤发生、血管生成、转移和 T 细胞免疫抑制(促肿瘤活性)。在 HCC 中,TAM 在临床结果中的作用仍存在争议,这可能是由于 TAM 的高可塑性和异质性。事实上,巨噬细胞可以分化为经典的(M1,镜像TH1)和交替的(M2,镜像TH2))。在功能谱连续体的极端情况下,巨噬细胞被激活。这些群体通常由诱导刺激(如CSF-< @1、M1 的 LPS 和 IFN-γ;M2的GM-CSF、IL-4和IL-13)),分泌特征(如IL-12高、IL-6高、TNFα高和M1高;IL-10高和TGF-β1高M2)、蛋白质标记(如M1的HLA-DR和NOS2;/MSR1/SR-A、/MRC1、/CSF-1R和M2 Arg1)和功能特征(例如,抗肿瘤或促肿瘤活性)和 CD68 是通常用于识别泛单核细胞/巨噬细胞的标志物。
在 HCC 中已经证明 M2 巨噬细胞可以通过产生 IL-1β 和 HGF 来改善 EMT 肿瘤转移,而 M1 巨噬细胞通过不同的整合素-Rho-通路抑制肿瘤转移。有趣的是,最近有报道称,索拉非尼在原位小鼠模型中通过 JAK 信号传导下调表达,从而诱导 EMT 并促进 HCC 细胞的侵袭和转移。
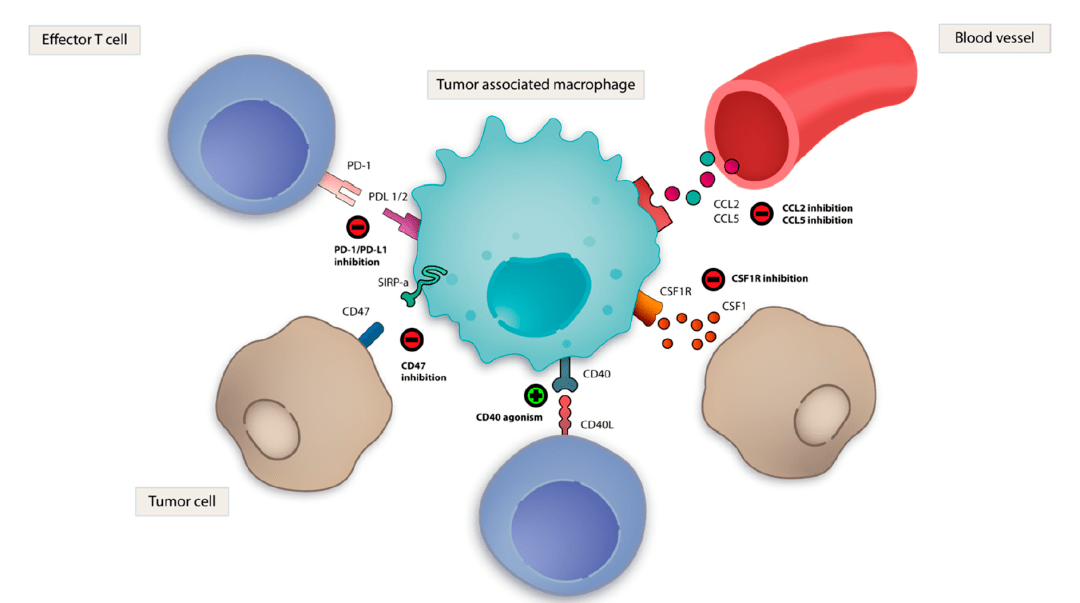
我们研究了 TAM 在 HCC 多吉美/索拉非尼耐药中的作用。索拉非尼有效抑制肝癌细胞的生长、集落形成和迁移。有趣的是,M2-CM显着降低了索拉非尼抑制肝癌细胞生长、集落形成和迁移的能力,而M1-CM则没有这种作用。
众所周知,TAM 会产生多种因子,其中一些因子,例如 IGF-1,可能会导致多吉美/索拉非尼耐药。通过筛选M1和M2巨噬细胞的差异基因表达,我们发现M2巨噬细胞大量表达HGF,而M1巨噬细胞分泌的HGF高出约30倍。用重组人 HGF 代替 M2-CM 降低了索拉非尼抑制肝癌细胞生长、集落形成和迁移的能力。M2-CM中加入抗-HGF消除了M2-CM对索拉非尼的活性,表明M2-CM中的HGF通过维持M2巨噬细胞的肿瘤生长和转移而赋予肝癌索拉非尼抗性起主要作用。除了与肿瘤相关的 M2 巨噬细胞外,与癌症相关的成纤维细胞和肝癌细胞也会产生大量的 HGF,这可能有助于获得索拉非尼耐药性。为了进一步探索潜在机制,我们评估了肝癌细胞中 HGF/c-Met、ERK/MAPK 和 PI3K/AKT 通路中关键蛋白的表达和磷酸化。我们发现对c-Met、ERK1/2和AKT的蛋白表达和pMet的磷酸化没有显着影响,但它显着降低了pERK/1/2和pAKT的磷酸化,证实了 抑制了ERK1/ 2/MAPK 通路通过靶向 RAF。M2-CM或重组HGF与索拉非尼的组合显着增加c-Met的表达和pMet、/2和pAKT的磷酸化;M2-CM和索拉非尼联合添加抗HGF抗体和索拉非尼单独使用具有相同的效果。总之,结果表明 (a) 索拉非尼本身不影响 HGF/c-Met 信号传导,但它通过靶向 RAF 抑制 ERK1/2/MAPK 信号,并通过 ERK1/2/MAPK 通路或其他机制抑制 PI3K/AKT 信号;(b) M2 巨噬细胞分泌的 HGF 激活 HGF/c-Met 信号传导和下游 ERK1/2/MAPK 和 PI3K/AKT 通路。事实上,PI3K 已被证明与 HCC 中的索拉非尼耐药有关。
在本研究中,我们发现HGF促进肝癌细胞和M2巨噬细胞的迁移,表明肿瘤相关M2巨噬细胞分泌的HGF可能会招募更多的巨噬细胞进入肿瘤并调节肿瘤组织中M2巨噬细胞的存在。在分布中,从而增加了肿瘤对肿瘤的抵抗力。索拉非尼前馈法。我们在裸鼠体内传代 HCC 细胞,用索拉非尼对小鼠进行诱导治疗,并将小鼠的肿瘤细胞再次植入小鼠体内,以进一步开发异种移植索拉非尼耐药和索拉非尼敏感性模型。我们发现 SR 肿瘤中 F4/80+/+ 双阳性 M2 巨噬细胞明显高于 SS 肿瘤。短期索拉非尼治疗可减少 F4/80+/+M2 巨噬细胞。但长期接触索拉非尼会增加HGF的合成和分泌,并增加 c-Met 和 pMet 的水平。由于索拉非尼也是一种抗血管生成剂,在某些情况下,抗肿瘤作用可能与抗血管生成活性、非肿瘤不良反应甚至肿瘤转移有关。我们通过 CD31 染色检查了 SR 和 SS 肿瘤中的肿瘤血管系统。SR肿瘤和SS肿瘤之间没有观察到内皮密度的显着差异,但SR肿瘤中的血管比SS肿瘤中的血管大,表明这种较大的血管也可能导致索拉非尼耐药。
总之,我们证明肿瘤相关的 M2 巨噬细胞代替 M1 巨噬细胞可以增加肝癌细胞的生长和迁移,并通过分泌 HGF 赋予对多吉美/索拉非尼治疗的抗性。M2巨噬细胞和肿瘤细胞的HGF激活肿瘤细胞内的HGF/c-Met、MAPK/ERK1/2和PI3K/AKT通路,从外周血循环中募集更多的巨噬细胞,调节M2巨噬细胞在肿瘤组织中的分布以前馈方式增加肿瘤对索拉非尼的抵抗力。我们的研究结果为多吉美/索拉非尼在 HCC 中的耐药性提供了新的见解,并提倡通过索拉非尼和强效 HGF 抑制剂(如卡博替尼)联合开发一线全身治疗,以提高一线疗效的新试验全身治疗。


