激酶药物发现的新趋势:新靶点、适应症和抑制剂设计
发布日期:2022-05-29 浏览次数:532
激酶药物发现的新趋势:新靶点、适应症和抑制剂设计(珍藏版)
2001 年 FDA 批准伊马替尼是分子靶向癌症治疗的一个突破,预示着激酶抑制剂作为肿瘤学及其他领域的关键药物类别的出现。二十年后,本文分析了针对激酶的已批准和实验性治疗的前景和趋势,包括最常用的激酶抑制剂靶点及其不断扩大的适应症。目前有 71 种小分子激酶抑制剂 (SMKI) 获得 FDA 批准,另有 16 种 SMKI 获得其他监管机构批准。尽管肿瘤学仍是其主要应用领域,但类风湿关节炎等适应症已获得大量批准,临床开发中的 SMKI 有三分之一涉及肿瘤学以外的疾病。 SMKI临床试验资料显示,目前正在探索约110种新型激酶作为靶点,而获批激酶抑制剂的约45种靶点仅占人体激酶组的30%左右,表明此类药物仍有很多未开发的机会。还讨论了激酶抑制剂设计的趋势,包括变构和共价抑制剂、双功能抑制剂和化学降解剂的开发。
背景
激酶和磷酸酶介导的可逆蛋白磷酸化在调节细胞功能(例如细胞增殖、凋亡、亚细胞易位、炎症和代谢作用)中至关重要。人体激酶组由约560种蛋白激酶组成,其中真核蛋白激酶(ePKs)约500种,分为酪氨酸激酶和非典型蛋白激酶约60种等8大类。
自 1980 年代以来,蛋白质激酶已被认为是潜在的药物靶点,尤其是基于对癌症的分子理解的进步,包括发现 SRC 等癌基因。然而,由于细胞内 ATP 浓度高、激酶活性调控机制知之甚少,以及一个保守的 ATP 结合口袋,开发与 ATP 位点结合的蛋白激酶抑制剂最初被认为是一项不可克服的挑战。
在 1990 年代,两种激酶抑制剂被批准用于临床。法舒地尔是 和 的抑制剂,于 1995 年在日本被批准用于治疗脑血管痉挛。西罗莫司是一种天然产物,在发现雷帕霉素的机制靶点 (mTOR) 中起关键作用,于 1999 年成为第一个在美国上市的激酶抑制剂,当时它被 FDA 批准用于器官预防排斥反应,第一个变构激酶抑制剂。鉴于这两种药物的历史,伊马替尼(CGP)——1992 年在 Ciba 实验室发现并于 2001 年获得 FDA 批准——被认为是激酶抑制剂开发的一个关键里程碑。伊马替尼可有效抑制多种酪氨酸激酶,包括 BCR-ABL 和血小板衍生生长因子受体 (PDF),最初被批准用于治疗 BCR-ABL 驱动的慢性粒细胞白血病 (CML)。其他适应症,如KIT驱动的胃肠道肿瘤(GIST)的治疗。
自 1995 年法舒地尔获批以来,全球获批的激酶抑制剂数量已增至 98 种药物,其中 71 种是 FDA 批准的 SMKI(截至 2021 年 5 月)。值得注意的是,在过去 5 年中,批准的 SMKI 数量增加了一倍以上,其中 37 种获得 FDA 批准,SMKI 约占 2016 年至 2021 年 FDA 批准的所有新药物的 15%。 10 种靶向受体酪氨酸的单克隆抗体 (mAb)激酶 (RTK) 也已获得 FDA 批准。其他 16 种 SMKI 和 1 种 mAb 已获得其他监管机构的批准。
图 1:批准的激酶抑制剂激酶家族和批准的药物靶点的时间表
FDA 批准 71 每个 SMKI 靶向 21 个激酶家族,约占激酶组的 20%,与之前对蛋白激酶靶标覆盖率的估计一致。已获得 FDA 批准(通常认为已通过行业标准进行临床验证)的药物靶向激酶包括 8 个主要 ePK 组(TK、TKL、STE、CMGC 和 AGC)中的 5 个家族成员,非典型蛋白激酶组(PIKK ) ) 和脂质激酶家族(PI3K;磷脂酰肌醇 4,5-二磷酸 3-激酶)。具体来说,这 71 种主要抑制这些组中的大约 42 种蛋白质,其中大多数(49 种)靶向 TK 组中 15 个家族成员的 30 种蛋白质(图 2)@ >。尽管 TK 组是最发达的激酶组,只有约 30% 被定位,表明仍有很大的进一步探索空间。
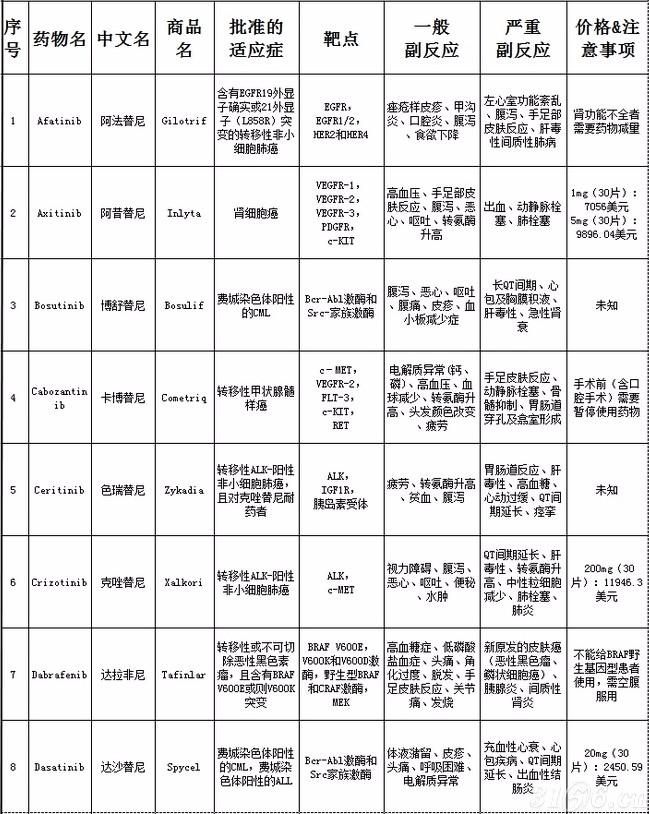
RTK 的 HER 家族成员(HER1-4)@ > 是最具针对性的,有 8 个 FDA 批准的 smk 和 8 个 FDA 批准的 mAbs 针对这些蛋白质。血管内皮生长因子受体 () RTK 家族也被目标广泛,有 7 个 FDA 批准的 smk 和 1 个 mAb,但所有 smk 都是非选择性抑制剂,并且还与其他 RTK 相互作用。激酶抑制 (JAK) 是另一种流行的治疗策略,迄今为止,针对这五种 SMKI 家族已获得 FDA 批准。
图2.DA 批准的肿瘤,其激酶抑制剂映射到人类激酶组激酶抑制剂
有大量临床证据支持激酶在癌症中的驱动作用,因为它们通过易位或激活突变异常激活。产生错误定位的融合蛋白的染色体易位可能是潜在的癌基因。大多数 FDA 批准的 SMKI (61; 89%) 和所有 FDA 批准的激酶靶向 mAbs (10 mAbs) 都有肿瘤适应症。在伊马替尼之后,迄今已批准 4 种 ABL 靶向 SMKI:尼罗替尼、达沙替尼、波舒替尼和波纳替尼。值得注意的是,CML 的治疗已被证明是持久的,相当一部分慢性期 CML 患者(高达 40 %)在停止治疗后没有复发。
超过 20%(19 种 SMKI 和 2 种 mAb)的获批药物已获批用于治疗非小细胞肺癌(其中肿瘤分子特征的鉴定使第一代SMKI的开发和应用成为可能,并指导进一步的药物开发以克服耐药性的出现。确实,针对获得性耐药 公司的下一代抑制剂占针对七个主要激酶基因家族的药物的 70%:NTRK、ABL、ALK、BTK、FLT3、KIT 和 MET。
在 2000 年代初获批用于吉非替尼和厄洛替尼的第一个 SMKI,其靶向表皮生长因子受体 (EGFR),基于其在肿瘤生长和进展中的重要作用。 44 然而,当靶向 EGFR 的 SMKI 时,通常会发生突变诱导的耐药性。尤其是在接受 EGFR 抑制剂治疗的患者中,高达 50% 的患者有管家突变。 FDA 批准的新一代 SMKI 对突变具有活性,选择性地靶向激活突变和抗性突变。新一代抑制剂奥希替尼也已获批。
靶向肿瘤 血管生成是一种重要的抗癌策略,许多已获批准的激酶抑制剂已成功针对不同适应症的 KIT、成纤维细胞生长因子受体 (FGFR) 和 MET 驱动的血管生成途径。例如,有五种 FDA 批准的 SMKI 被批准用于抑制肾细胞癌和其他 RTK,以及两种批准的靶向抑制剂,即西罗莫司和依维莫司。
其他 RTK 蛋白家族已被批准用于各种癌症适应症的激酶抑制剂。其中最突出的是针对乳腺癌的 HER2 靶向药物,该数据集包括九种已批准的激酶靶向药物。其中包括 1998 年批准的 HER2 靶向 mAb 曲妥珠单抗,它提供了在伴随诊断指导下使用 RTK 靶向药物的开创性例子。各种细胞内激酶也被批准的 SMKI 靶向。靶向在细胞分裂中起重要作用的 CDK4 和 CDK6 已经非常成功,其中三种现在已成为标准疗法,尤其是针对乳腺癌适应症。
靶向激酶在治疗其他血液系统恶性肿瘤方面取得了实质性进展。值得注意的是,三种获得 FDA 批准的酪氨酸激酶 (BTK) 抑制剂正在用于治疗套细胞淋巴瘤和慢性淋巴细胞白血病。
已批准的肿瘤外激酶抑制剂
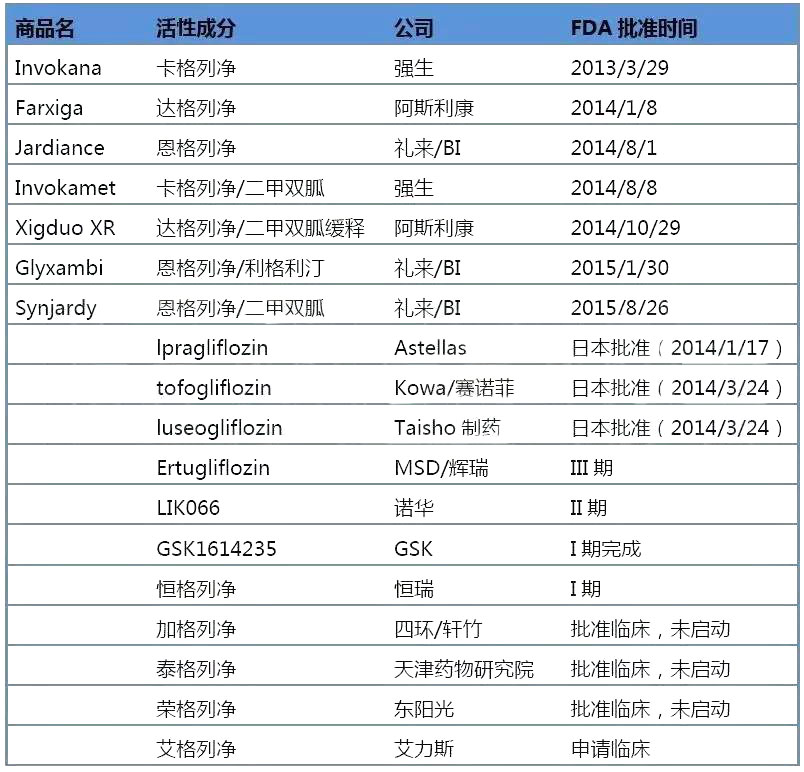
许多激酶参与免疫反应的调节。例如,JAK 是 T 辅助细胞(TH1、TH2 和 TH17))免疫反应的关键成分,因为它们是许多细胞因子(包括干扰素和白介素)的第二信使。 11 种 SMKI(占已批准 SMKI 的 13% 以上)已被批准用于免疫系统相关适应症,主要是自身免疫性疾病和炎症性疾病。
FDA 于 2011 年批准了第一个 ,一种在肿瘤学之外获得批准的激酶抑制剂,是 JAK1 和 JAK2 的抑制剂,用于治疗中度或高危骨髓纤维化患者。一种 JAK2 抑制剂也于 2019 年获批用于此类疾病。
类风湿性关节炎是一种自身免疫性疾病,其中批准最多的 SMKI(总共 5 个,3 个 FDA 批准)。所有 5 种 SMKI 均选择性靶向 JAK 亚型,包括 2012 年批准用于类风湿性关节炎的第一个 SMKI(托法替尼),其次是 、 和 .主要抑制JAK3,2019年获日本药品医疗器械管理局(PMDA)批准。然而,出于安全原因,FDA 推迟了对新药申请的决定。 JAK激酶抑制剂也在针对其他免疫疾病进行研究,是一种泛JAK抑制剂,于2020年获得PMDA批准,是首个获批用于特应性皮炎皮肤病的激酶抑制剂。
参与先天性和适应性免疫反应的激酶SYK与过敏性和自身免疫性疾病以及血液系统恶性肿瘤的发生密切相关。一种一流的 SYK 抑制剂,由于能够减少抗体介导的血小板破坏,于 2018 年被 FDA 批准用于慢性免疫性血小板减少症。器官移植和移植针对宿主疾病的排斥预防也是适用于激酶抑制的免疫相关问题。两种药物依鲁替尼和鲁索替尼已分别获批用于治疗这些疾病。
已批准激酶抑制剂的化学趋势
ATP 结合位点是已获批准的 SMKI 靶向的主要位点,占 FDA 批准的 71 种药物的 63%。与 ATP 腺嘌呤环类似,ATP 模拟抑制剂通过氢键锚定在激酶铰链骨架上。已经开发了几种支架作为铰链粘合剂(图3)融合六元环系统,例如(异)喹啉和喹唑啉,首先在法舒地尔的开发中建立,其次是吉非替尼和厄洛替尼,是最常用的ATP 模拟物与 18 个批准的 SMKI。用于伊马替尼的氨基嘧啶和密切相关的氨基吡啶部分也仍然是常用的铰链结合剂,有 17 个批准的 SMKI。
第三组铰链结合基团是稠合的五元和六元环系统,例如吡咯并嘧啶和吡咯并吡啶、嘌呤、羟吲哚和吡咯或咪唑三嗪。在结构上,吡唑氨基嘧啶和咪唑氨基吡嗪也与这类铰链结合物有关,但基于其铰链结合方式,应认为是氨基嘧啶的衍生物。非芳香铰链结合基序由羧酰胺代表。共有 17 个 SMKI 包含不同的铰链结合支架,但在开发三分之二已获批准的 SMKI 中所探索的狭窄化学空间令人震惊。
图 3:已获批准的激酶抑制剂中使用的化学支架的临床试验趋势
在临床试验中注册的激酶靶向药物近600种,其中新型SMKI 475种,生物制剂124种。在临床试验中注册的 475 种 SMKI 中,近一半(253 种)目前正在开发中,包括正在进行的试验或开始新的试验,而 222 种被确定为未在积极开发中。临床试验中约 40% (194)@>) 的激酶抑制剂靶向 45 个新激酶家族,包括 215 种蛋白质(40% 的激酶组),尽管我们确定其中约 110 种为主要激酶抑制剂靶标,因此更准确估计有 20% 的激酶组超出已获批准药物的验证靶标,正在与处于临床开发阶段的药物进行研究(图 2)1@>。
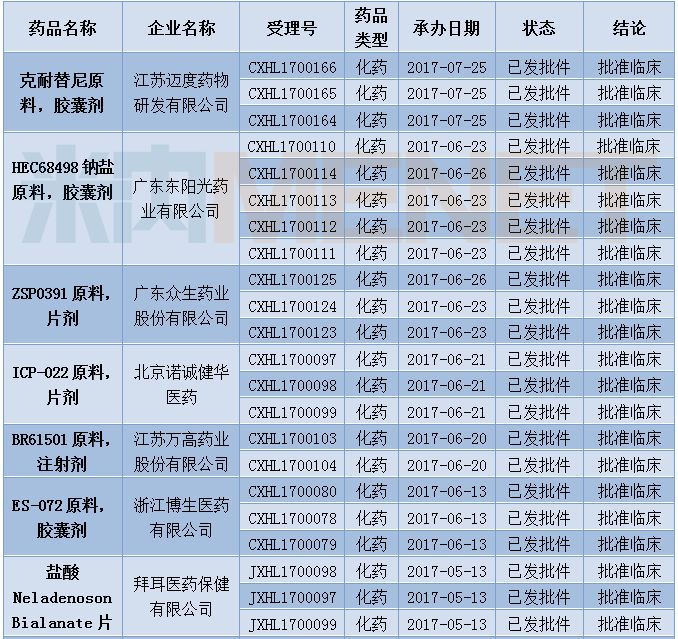
2)2@>
图2)3@>针对新型激酶家族的药物临床试验时间表
如上所述,临床试验中至少有 45 种不同的新型激酶家族,其中包括 110 多种不同的激酶被确定为主要目标。一些家族已成为临床开发中大量药物的目标,抑制剂在化学和靶向适应症方面经历了演变。有趣的是,与其他主要激酶相比,新型家族在 TK 组中的靶向性低于 TK 组。在CMGC(CDK、MAPK、GSK3和CLK家族)组中,有近50种药物已进入临床试验长期研究的成员,如丝裂原活化蛋白激酶(MAPK)p38家族、ERK家族和依赖性激酶 (CDK) 家族成员。超过 20 种药物靶向激酶家族,而在 AGC 组中,17 种抑制剂靶向 AKT(蛋白激酶 B,PKB)家族。下图总结了激酶靶向药物在临床试验中的疾病适应症。
图2)4@>激酶靶向药物临床试验适应症总结
尽管激酶药物发现取得了重大进展,但该领域仍存在许多挑战和机遇。在肿瘤学领域,自伊马替尼获批以来的二十年里,激酶抑制药物已成为癌症治疗的基石之一,而对抗耐药性对于长期疗效至关重要,目前正在制定几种此类策略。针对常见和罕见激酶驱动突变的药物设计用于对抗耐药性 如上所述,一种方法是开发多代激酶抑制剂。使用联合治疗方案是另一种方法,如在黑色素瘤治疗中使用 BRAF 和 MEK 抑制剂的组合所示。此外,具有多种激酶抑制作用的单分子抑制多种相关激酶的合理开发也很有希望。
还存在功能性挑战,例如癌症激酶组中基因异常的表征,以及确定导致肿瘤发展的真正驱动因素。仔细分析激酶的生物学途径及其与细胞生物学和治疗干预的关系非常重要,因为激酶在非恶性细胞中可能是肿瘤抑制因子,但在肿瘤存活的恶性细胞中起介导作用。
为了继续扩大激酶药物发现,需要进一步开发和完善有效的化合物筛选和分析技术。特别是,需要解决可以识别新化学物质(包括天然化合物)的方法。此外,还存在于实现目标选择性以减少脱靶毒性挑战。开发具有不同类型结合模式的抑制剂,例如变构和共价抑制剂,以及靶向降解剂和分子胶,可能在未来二十年的激酶药物发现中发挥关键作用。
本文为 AIDD Pro 接受的外部投稿。本文所表达的观点仅代表作者自己的观点,不代表AIDD Pro平台。如发现发布内容中存在侵犯版权或对其他信息的误解,请及时联系AIDD Pro进行删除和修改处理。
参考文献
, M.M., , D., , A.V.等。在药物中: 和 。 Nat Rev 药物 (2022)5@>.


