一下奥希替尼的耐药问题有哪些方法?来自草根的解读
发布日期:2022-02-01 浏览次数:268
结合过去一年的研究和患者的实际情况,我们来盘点一下奥希替尼的耐药情况。有一些方法,从草根开始。
1、发现有耐药趋势,有什么办法可以延缓复发?
靶向耐药不是一天就能达到的,所以我们需要抓住一开始就有迹象的时间段,做一些事情来延缓全面复发。患者常有咳嗽、胸痛等新症状,或症状日益加重,或定期复查中的肿瘤标志物癌胚抗原(CEA)持续升高,复查影像病灶可能无变化,略有增加,等等,可以称为“慢”。抵抗”阶段。
对于这个有耐药趋势但没有实质性确定耐药性的时期,我们可以采取一定的措施来延缓耐药性,给出几种方案:
1.增加奥希替尼的用量,最多可达
临床上使用的药物都具有一定的量效正相关关系,即剂量越大疗效越好,但副作用当然会增加,而我们每天使用的剂量是疗效和毒性之间最好的. 平衡点。但这也意味着增加剂量可以在一定程度上提高药物的疗效。这在一些小样本研究中进行了比较,有效率高于80mg(87% vs 67%)[1]。
美国国家综合癌症网络 (NCCN) 指南中推荐使用奥希替尼治疗最难治性脑膜转移瘤,因此也表明该剂量是身体可以耐受的。这种缓解方法常用于许多基层患者,具有一定的拖延倾向。但延迟时间因人而异。
2.奥希替尼加化疗
耐药的本质是体内对奥希替尼敏感的细胞减少,而其他类型的细胞成为主要原因。杀死所有细胞的化学疗法可以在您不知道自己拥有哪种类型的细胞时帮助您稳定病情。对此,国内肺癌专家、上海交通大学附属胸科医院韩宝辉教授[2]进行了一项随机对照研究,将99名患者随机分为两组:一组处于缓慢耐药阶段。 EGFR靶向药物,在靶向的基础上,增加化疗和靶向联合模式;二是在耐药缓慢阶段继续使用单药靶向,待明确进展后替代靶向序贯化疗。结果显示,联合模式的无进展生存期(PFS)优于序贯模式(7.7vs5.7个月);即使在总生存期(OS)方面,联合组也明显更好地延长了(0.7个月),死亡风险降低了48%。
甚至有很多患者会在靶向治疗有效的情况下间歇性地接受化疗。抑制“不安分”的异种细胞。对此没有研究支持,仅供个人参考。
3.奥希替尼加抗血管药物如贝伐单抗、安罗替尼、阿帕替尼(出血患者慎用)
抗血管药物可以调节肿瘤病灶内紊乱的血管,使药物更好地进入肿瘤深部,从而增强疗效。国内学者在2020年欧洲医学肿瘤学会(ESMO)大会上进行的一项小型临床研究表明,在奥希替尼耐药后,加用阿帕替尼的PFS比直接替代化疗延长了2倍以上(10.5vs4.5 个月)。
当然,在耐药期间,有经济实力的患者可以开始第二轮基因检测。
2、如果我有明确的耐药性怎么办?
以上操作会延迟一定时间的无复发时间,但很难长期保持。因此最终会进入耐药阶段,即CT明确提示病灶明显扩大或出现新病灶。在这个阶段我们做什么?
首先,做一个快速的基因测试(血液测试更快,组织测试更准确)。需要提醒的一件事是,基因测试的结果需要 1-2 周才能出来。这段时间,不要闲着。大多数临床医生会推荐化疗。如果化疗没有被拒绝,体质可以接受的患者,确实应该接受积极的化疗。. 当然,靶向治疗组中的一些患者对化疗非常耐药。对于此类患者,现阶段可以采用针对性+模式,如上述模式。一句话,别等了。
1.主要病灶尚有效,但有寡转移灶,可继续靶向+放疗对新转移病灶
什么是“寡转移”,寡转移是指少数,1-2个新的转移灶,如转移到脑、骨、肾上腺等;但是还有一个很重要的前提,主要病灶还是有效的,比如肺部病灶没有增加,稳定或者还在缩小,但是有新的转移灶。在这种情况下,可以采取局部治疗新病灶的思路,在继续靶向治疗的前提下,对寡转移病灶进行局部放疗。这在指南中得到了同意。
2.基因检测显示患者存在二次突变
在奥希替尼耐药患者的基因检测中,二次突变是常见的耐药突变,占15%-20%。分为顺势突变和反式突变,多为顺势突变。对于/突变的患者,可以采用奥希替尼+吉非替尼,即第三代+第一代治疗方案。然而,对于具有/顺势突变的主要耐药人群,需要西妥昔单抗+布加替尼。下图是顺势疗法耐药患者的治疗案例。
患者62岁女性,接受化疗-第一代EGFR靶向治疗-奥希替尼治疗-奥希替尼耐药-发现/顺势突变-布加替尼(90mg/天)+西妥昔单抗西昔单抗(/月),治疗一个月后,患者呼吸困难明显好转,病灶缩小。
当然,还有其他类似的对第三代靶向药物不敏感的二次突变基因,如,等,也可以根据敏感性谱,通过1-3代组合解决。
3.基因检测发现MET扩增
MET扩增是EGFR靶向耐药的常见原因,占10%-15%,也是奥希替尼耐药患者常规检测的靶点之一。如果检测到MET扩增,可以采用奥希替尼+MET抑制剂的方法治疗(可以用克唑替尼,也可以找卡博替尼的仿制药;西沃替尼即将在中国上市,届时可以优先考虑)时间。萨瓦替尼)。
以下患者在奥希替尼耐药后发现MET扩增,再次出现耐药后给予奥希替尼+克唑替尼、卡博替尼+奥希替尼治疗。
4.其他旁路基因激活的基因检测
在对奥希替尼耐药的患者中,也可以检测到其他基因的旁路激活,如HER2、BRAF、ALK,占比较小,但目前已有实际案例。一旦检测到,可以采用EGFR靶向药物+旁路基因抑制剂的组合方案进行治疗。
5.耐药性也可能是由于小细胞转化
在我们长期用药的推动下,肺癌也可能发生病理转化,比如从肺腺癌或肺鳞状细胞癌转化为小细胞肺癌,或部分转化。如何发现?参考终点的方式有以下三种:(1)肿瘤标志物中的神经元特异性烯醇化酶(NSE)指数异常升高;(2)基因检测发现RB1和TP53突变;(3)其他病灶对治疗有效,唯一的病灶(可以是新病灶)出现异常扩大,其生物学行为与其他病灶不同。在这三个案例中,存在高度怀疑 SCLC 转化的可能性。当然,最终确认仍需病理活检。一旦确定了转化,就将处理与 EP/IP 相结合,
6.如果没有发现继发耐药的突变基因,化疗是首选,单独免疫也不是很好的选择
虽然我们的靶向免疫发展如火如荼,但对于奥希替尼耐药,在没有继发耐药基因的情况下,坦白严肃地说,化疗是首选,也是迄今为止最有效的治疗方法。. 腺癌患者采用培美曲塞+卡铂±贝伐单抗,鳞状细胞癌患者可采用吉西他滨/紫杉醇+铂治疗。当然也可以采用化疗联合PD-1单克隆抗体,有效率可达50%。
有人问,用PD-1/PD-L1单克隆抗体免疫治疗可以吗?在没有强有力的原因(例如高 PD-L1 表达和高肿瘤突变负荷(TMB))的情况下,不推荐单独使用免疫治疗,因为它可能无效且过度进展。
7.PD-1/PD-L1免疫+抗血管安罗替尼/阿帕替尼
由于单独的免疫疗法有风险,因此可以使用联合免疫疗法。免疫+抗血管的组合对多种癌症都有效,甚至在肺癌一线,在小样本初步结果中也取得了不错的效果。因此,也被人们用来挑战奥希替尼耐药问题。有很多成功的案例和临床研究数据。但是,我也看到过这种方案仍在快速进展的患者无效,而且它不是灵丹妙药。
2020年6月,中国学者发表了PD-1单克隆抗体联合抗血管药物治疗晚期非小细胞肺癌的真实世界临床研究结果。总体缓解率为31.9%,疾病控制率(DCR)为89.9%。其中EGFR突变患者16例。这16例患者靶向耐药后PD-1单克隆抗体联合抗血管的有效率为18.8%。
8.改用其他治疗,以后还可以改回奥希替尼
在没有可用的靶向药物的情况下,对奥希替尼耐药的患者理论上应该接受阳性结果的化疗。一些研究发现,化疗可以使患者对靶向药物再次敏感。一项研究回顾性分析了 17/21 名突变患者,既往治疗线的中位数为 5,奥希替尼挑战的客观缓解率(ORR)(15 名可评估疗效的患者)为 33%,DCR 为 73%。另外两名患者接受了奥希替尼治疗癌性脑膜炎(由肿瘤脑转移引起),其中一名患者的头痛和恶心等症状得到了显着缓解。
9.双抗体药物JNJ-6372+第三代EGFR-TKI药物
这个计划是后来写的,不是因为效率不高,而是目前国内没有上市,但是有临床试验可以参与,患者可以积极寻求参与。这是一个非常新颖的想法。JNJ-6372是一种针对EGFR和MET的双抗体药物。每个人都不熟悉它。可以简单理解为奥希替尼的兄弟。因此,这种药物组合基本上是MET通路抑制剂+西妥昔单抗类药物+奥希替尼的组合,三种靶向力量共同作用。结果真的很好。
在 ESMO 2020 报告的研究中,该组合用于治疗对奥希替尼耐药的患者。在 45 名患者中,总反应率为 36%,DCR 为 60%。16例病情缓解的患者中,14例仍在临床治疗中。
3、未来可能的希望
1.EGFR突变,第一代+第三代
这是2020年美国临床肿瘤学会(ASCO)会议上发布的一项新思维测试,主要基于“三代耐药后的二次突变对一代敏感,一代耐药后的突变对三代敏感”几代人”。换句话说,肿瘤细胞在我们的药物之间跳跃,第一代和第三代相互替换。那么如果直接用1代+3代从头开始挡住它的跳跃方式,会不会延长有效时间呢?
一些学者沿着这条路线设计了临床试验,但在ASCO会议报告时数据还没有完全成熟。从影像学评估的缓解状态来看,88.9%的病灶缩小,达到客观缓解;所有病例(100%)均实现疾病控制,其中部分缓解24例,病情稳定3例。报告时 PFS 和总生存期 (OS) 数据不成熟。中位随访时间为 15.3 个月,33% 的病例达到 PFS 终点,估计中位 PFS 为 22.5 个月。
同时检测循环肿瘤DNA( ),发现联合治疗2周后88%(15例)患者血清EGFR+检测不到,清除率几乎100%。随访至第8周,未检测到EGFR+。这表明持久和完全的血浆 EGFR 清除几乎只发生在 EGFR-TKI 联合治疗下。
因此,我们期待本研究后续成熟的数据报告,或许会开创一种新型的治疗思维!
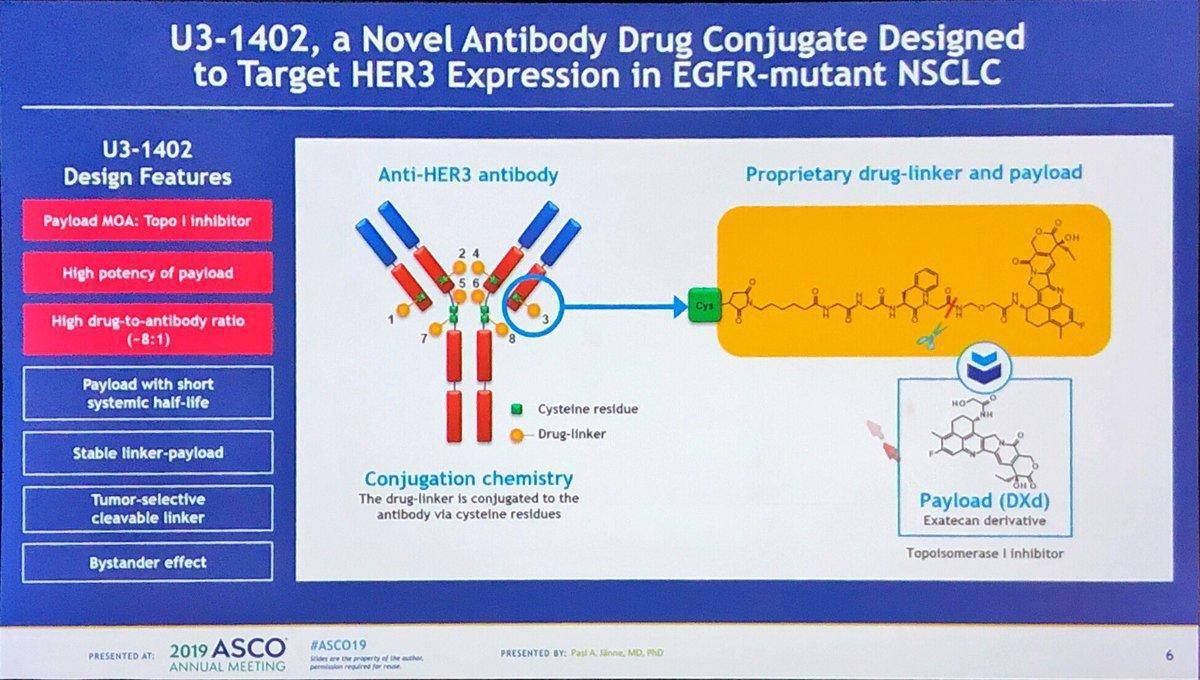
2.HER3 mAb U3-1402
EGFR也被称为HER1,HER3是HER1-4家族的成员。近两年,逐渐被发现有药用价值。U3-1402 是一种靶向 HER3 的抗体药物偶联物 (ADC)。在一项对 57 名既往接受过 EGFR-TKI 治疗的 EGFR 突变肺癌患者进行的研究中,86% 接受过奥希替尼,90% 接受过铂类化疗,40% 接受过免疫治疗。人数为 4,其中 27 人(27%)有脑转移。所有患者每三周接受一次 U3-.6 mg/kg。总有效率为25%,%,中位缓解持续时间为6.9个月。在具有突变、突变、MET基因扩增、HER2突变、BRAF融合和突变的患者中观察到部分肿瘤反应。因此,该药很有希望成为解决奥希替尼的新药。
3.两种有前途的第四代EGFR靶向药物
在过去2020年世界知名会议上报道的药物中,有3种被称为第四代EGFR-TKI的药物已经展现出巨大的潜力,值得期待。
(1)BLU-945是第四代EGFR-TKI药物,专门针对奥希替尼耐药原因/共突变和其他T90M耐药突变。研究结果表明,从使用奥希替尼的小鼠模型中对BLU耐药的非小细胞肺癌患者的//突变肿瘤细胞株进行异种移植,BLU-/kg,每天两次,口服,肿瘤明显缩小。
(2):2020年,美国癌症研究协会(AACR)报道了第四代共突变靶向药物,其分子式近日公布。如前所述,二次突变主要是Oxi替尼的耐药机制,约占21%。它是一种ATP竞争的非共价抑制剂,与EGFR的αC--in构象结合。体外肿瘤细胞系和小鼠实验表明,/,/, // 和 // 突变都具有显着的肿瘤抑制作用。


