2022年第53届美国妇科肿瘤学会召开II期单臂临床研究
发布日期:2022-03-24 浏览次数:275
2022年第53届美国妇科肿瘤学会(SGO)将于3月18日至21日在美国亚利桑那州凤凰城以线下+线上的方式召开。该研究是序贯尼拉帕尼联合贝伐单抗的II期单臂临床研究晚期卵巢癌患者一线铂类化疗联合贝伐单抗后的维持治疗。此前,在 2021 年 SGO 大会上宣布了其 62% 的 18 个月无进展生存期( PFS )率。本次会议上,研究人员公布了中位PFS、总生存期(OS)、至首次随访治疗或死亡时间(TFST)、至第二次随访治疗或死亡时间(TSST)、安全性等数据的更新研究.
研究背景
根据 /-OV26/GOG-3012 研究,PARP 抑制剂 被批准用于铂敏感、晚期或复发性卵巢癌患者的单药维持治疗,无论 HRD 状态如何。GOG-218 和 ICON-7 研究表明,标准化疗加贝伐单抗可以改善卵巢癌患者的 PFS。该研究旨在探讨尼拉帕尼联合贝伐单抗维持治疗在新诊断的晚期卵巢癌患者中的安全性和有效性,无论生物标志物状态如何。
研究方法
纳入标准为新诊断的高级别浆液性或子宫内膜样III-IV期卵巢癌、输卵管癌或原发性腹膜癌,在一线含铂化疗联合贝伐单抗后完全缓解(CR),部分缓解(PR)或没有疾病进展的证据,以及既往接受过新辅助化疗或原发性细胞减灭术的患者。
患者在入组时完成了同源重组 (HR) 组织检测。患者接受 200 或 QD(基于体重/血小板计数)+ 贝伐单抗 15 mg/kg Q3W。在完成 3 年的一线治疗后 12 周内开始尼拉帕尼,或直至疾病进展/不可耐受的毒性;接受贝伐单抗≤15个月(包括一线化疗的持续时间)。该研究的主要终点是 18 个月的 PFS 率。次要终点包括 PFS、OS、安全性、耐受性和 FOSI 评分相对于基线的变化(图 1).
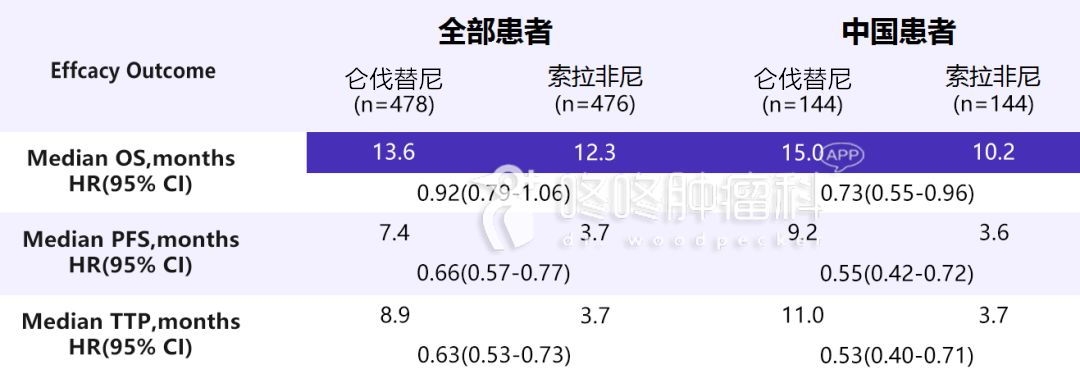
图1 实验设计
研究成果
本研究共纳入 105 例患者,患者基线特征见表 1。
表 1 患者的基线特征
中位随访时间为 28.7 个月(IQR,23.9-32.5)。在总体人群中,中位 PFS 为 19.6 个月(95%CI,16.5-25.1),操作系统不成熟,操作系统事件率 23.8%,TFST 为 17.5 个月 (95%CI, 14.5-20.7), 未达到 TSST (95%CI, 32.1- NE)。与同源重组修复功能正常(HRp)(14.2个月[8.6, 16.8])和同源重组修复功能不确定(HRnd)亚组(12. 1 个月[8,NE]) 与同源重组修复缺陷 (HRd) 亚组 (28.[19.9] , NE]) 相比具有更好的中位 PFS (95%CI) (图2). HRd/BRCA 野生型患者的中位 PFS(n=16) 为 28.3)。个月 (95%CI, 12.1-NE),而 HRd/BRCA 突变患者的中位 PFS (n=29) 未达到 (95%CI, 19. 3-NE)。
图2 PFS分析
在安全性方面,与已知的尼拉帕尼和贝伐单抗单药治疗的安全性特征一致,没有观察到新的安全性信号(表 2).
表 2 不良事件
FOSI 基线平均 (SD) 得分为 25.7 (3.79) 和最小二乘平均从基线变化 -0.7 (0.@ >35)(图 3).
图表分数
分析结论
尼拉帕尼联合贝伐单抗在一线含铂化疗后仍可观察到疗效,FOSI评估结果显示联合治疗对患者生活质量无明显影响。
参考:
M. , , 盖尔 S. 等人。2 of + in - with 。2022 年


